オーストラリアで実施された脳性麻痺に対する自家臍帯血投与の安全性と実現性を示した初症例が報告されました

オーストラリアより、脳性麻痺児に対する自家臍帯血の投与が、同国の未承認医療アクセス制度であるSAS(Special Access Scheme)を活用して実施され、その初症例が報告されました。
脳性麻痺は、胎内または周産期に生じた脳損傷に起因する永続的な運動障害であり、根本的な治療法は限られています。近年、臍帯血を用いた再生医療の可能性が世界的に注目されており、特に自家臍帯血投与による運動機能改善の可能性について、複数の臨床研究データが蓄積されてきました。
SASは、未承認医療を患者ごとに個別審査のうえ実施できる制度であり、特例的に治療へアクセスできる仕組みです。今回の症例では、これまでに報告された国際的な臨床研究のエビデンスを基に、オーストラリア医薬品行政局(TGA)の承認を受け、SAS制度を通じて自家臍帯血が投与されました。本報告は、脳性麻痺に対する自家臍帯血投与がSASを用いて実施された初の症例報告となります。
今回の報告は、制度を活用することで未承認治療へのアクセスが可能となることを示したものであり、今後オーストラリアにおける臍帯血治療の選択肢拡大につながる可能性があります。一方で、現在の規制の枠組みでは海外からの患者受け入れは想定されておらず、国外患者が同制度を利用することはできません。将来的に制度の運用や規制が見直された場合には、海外患者に対する治療アクセスの可能性が広がることも期待されます。
SASについて
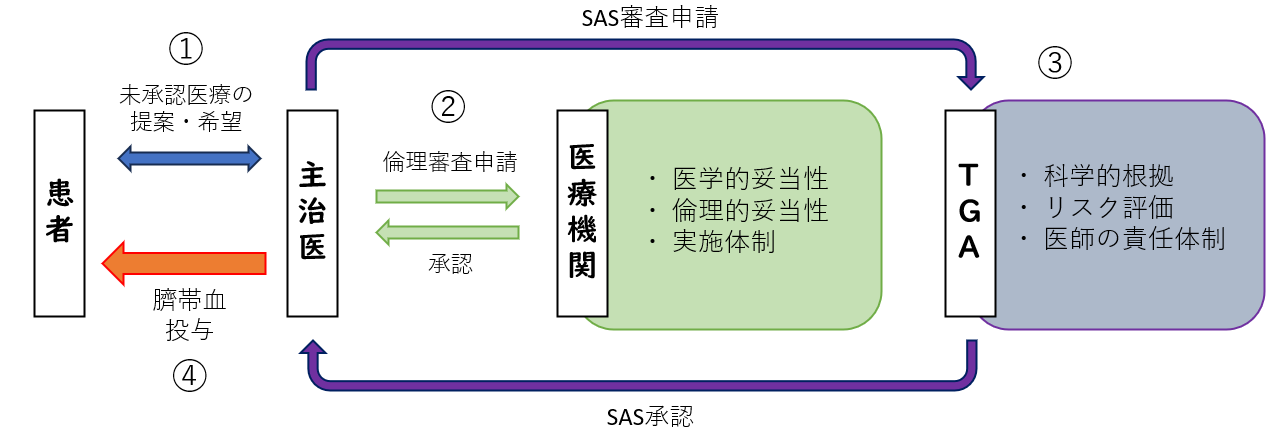
SASは、オーストラリアにおいて、未承認医療を患者ごとに個別審査のうえ使用できるアクセス制度です。治療法そのものを承認するものではなく、医学的妥当性が認められた場合に限り、特定の患者に対して特例的に実施が認められます。
実施にあたっては、以下の流れで手続きが進められます。
① 主治医から未承認医療の提案、または患者・家族からの希望をきっかけに検討が開始
② 主治医が医学的妥当性を整理し、医療機関内の倫理委員会等で実施の妥当性を審査
③ 主治医がTGAへSAS申請を行い、規制当局による個別審査
④ 承認後、適切な管理体制のもとで投与を実施
未承認医療であることから厳格な審査体制が設けられていますが、この仕組みにより、医学的妥当性が認められた場合に限り、治療への道が開かれています。
本症例について
本症例は、5歳の脳性麻痺女児に対して自家臍帯血を投与したケースです。
本児は、脳性麻痺の運動機能の重症度を5段階で分類する尺度であるGMFCS(Gross Motor Function Classification System)レベルIIに該当していました。GMFCSレベルIIは歩行は可能であるものの、走行やジャンプなどの高度な運動に制限がみられる段階を指します。
昨年5月発行のHOPECELL NEWSでもご紹介した、脳性麻痺に対する臍帯血治療の有効性を支持する研究論文の結果を踏まえ、本症例でも治療効果が期待される条件を満たすことが確認されました。こうした国際的なエビデンスを基に、SAS申請が行われています。
投与前には、臍帯血との適合性を確認する検査(HLA検査)や血液検査が行われ、いずれも問題は認められませんでした。使用された臍帯血は、無菌性や細胞の生存率などの品質確認を経て洗浄された後、総細胞数 42.7×10⁶/kg が静脈内に投与されました。
投与は問題なく終了し、健康被害などは認められませんでした。投与後は4時間のモニタリングが行われ、念のため一泊入院で経過観察を行った後、翌日問題なく退院しました。
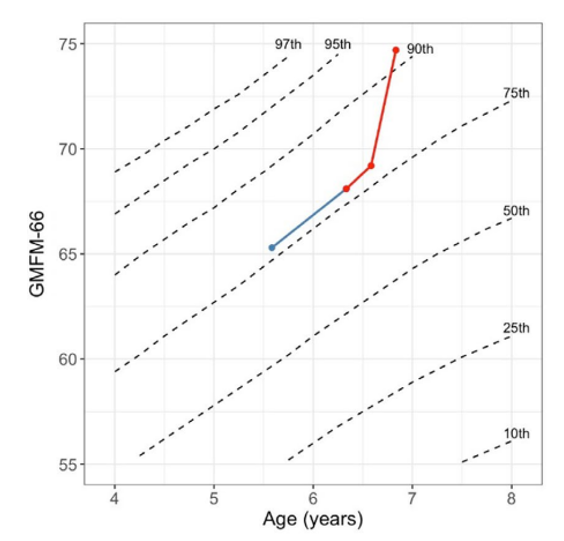
(上図)図1A
臍帯血投与前後におけるGMFM-66スコアの推移
運動機能は、立位や歩行、走行、跳躍などの粗大運動能力を点数で評価する指標であるGMFM-66(Gross Motor Function Measure)により評価されました。
図1Aは投与前後のスコアの推移を示したグラフで、点線は同じGMFCSレベルIIの子どもたちにおける年齢に伴う一般的な運動機能の推移を統計的に示した基準線です。青線が投与前の経過、赤線が投与後の経過を示しており、本症例のスコアはこの基準線と比較して投与後に明らかな上昇を示しました。投与時の68.1から、投与後3か月で69.2、6か月で74.7へと改善し、合計6.6ポイントの向上が認められました。
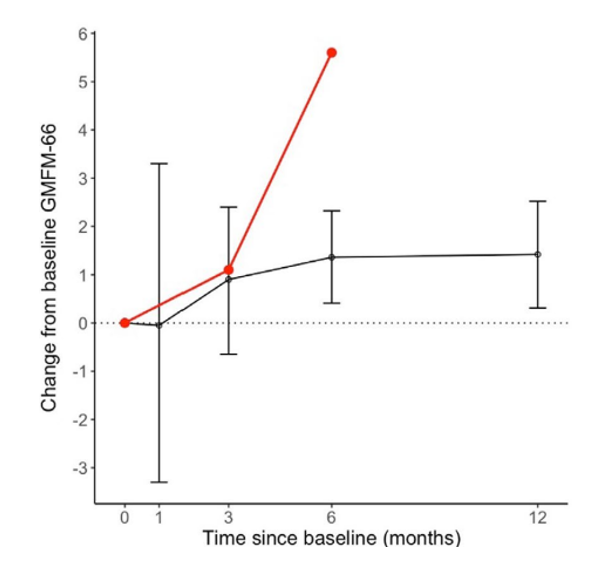
(上図)図1B
GMFM-66スコア改善量の既存研究データとの比較
図1Bは、投与時からの変化量を過去の臨床試験データの平均改善量と比較して示したグラフで、本症例の改善幅は過去の試験データと同等以上の水準で推移しており、粗大運動能力の悪化は認められませんでした。
臨床的にも、複数の課題において運動の質と運動制御の改善が認められました。作業療法士による臍帯血治療前および治療後5週目・8週目の機能評価では、「鬼ごっこ」中の転倒回数が6回から0回へと減少しました。これは移動能力における実生活での改善を示しています。また、疲労感の軽減も確認されました。
本報告では、GMFMスコアが投与6カ月で6.6ポイント改善しました。高知大学によるフェーズⅠ試験では、GMFMスコアが投与1年で5.0±3.3ポイント改善し(Kikuchi et al., 2017)、Duke大学によるフェーズⅡ試験では投与1年で7.5±6.8ポイントの改善が報告されており(Sun et al., 2017)、本症例においても同様の改善傾向が認められました。大規模な臨床試験の実施が容易ではない現状において、SASのような制度を活用した症例の蓄積は、臍帯血投与への現実的なアクセス手段となり得ます。なお、現行の規制の枠組みでは海外からの患者受け入れは想定されておらず、日本を含む国外患者が本制度を利用することはできません。将来的に制度の運用や規制が見直された場合には、海外患者に対する治療アクセスの可能性が広がることが期待されます。